背景介绍
单细胞RNA测序技术(scRNA-seq)凭借其非偏向性检测和大规模并行分析优势,成为解析异质性细胞群体特征的有力工具。BD Rhapsody™ 单细胞分析系统配备的专有单细胞捕获技术,以微孔为基础,能够捕获成千上万个单细胞并为其打上条形码,以分析转录组和蛋白质组信息。BD Rhapsody™ HT 单细胞分析系统可以灵活地处理样本和捕获细胞(从数百个到上百万个单细胞),自然沉降的微孔板技术对细胞温和而无损伤,增强型磁珠的多级条码技术,确保实验强健而稳定。利用碧迪医疗多样本标签,可在一次运行中处理多个样本。捕获的细胞信息被用来构建各类文库,通过二代测序,加速探索更多研究发现。
技术优势
1、强大的样本兼容性
细胞活性>50%即可上机、对细胞背景宽容、Scanner质控系统加持、可以进行肺泡灌洗液、植物原生质体、海洋泛模式生物等脆弱类型细胞的上机实验。
2、卓越的粒细胞捕获能力
BD稳定捕获高比例粒细胞具有更优的基因中值,适用于中性粒、嗜酸粒、嗜碱粒等细胞的捕获。在肿瘤、风湿、感染、血液病等疾病具有广阔应用场景。
3、灵活的细胞通量
具有8个通道,互相独立,每个通道可捕获100-60000个细胞,100%利用效率,显著降低单细胞成本。
4、强大的多组学平台
可以同时获取单细胞层面上转录组、蛋白组、VDJ、ATAC的信息,具有稳定的混样技术、可以消除批次效应、节约成本
技术路线
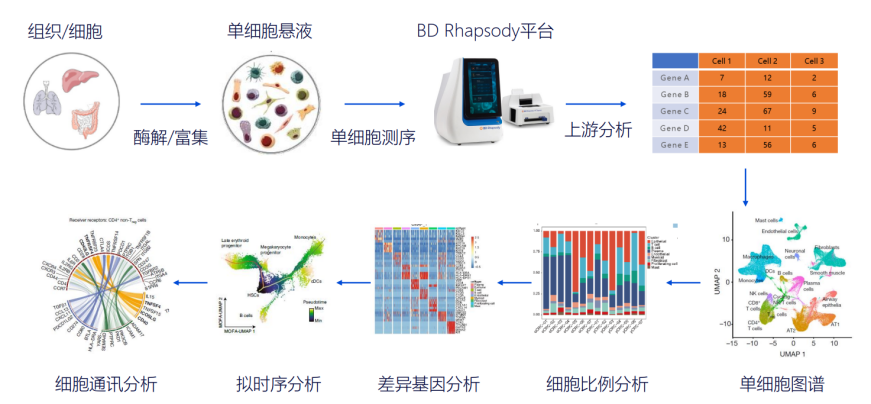
样本要求
|
样本类型 |
样本量及保存条件 |
|
实体组织 |
≥0.2g(参考黄豆粒:0.5 cm2大小),组织样本于充满预冷组织保存液(免费提供)的螺口冻存管中,密封后于 2-8°C 保存/运输; |
|
⾎液,骨髓类样本 |
≥2mL ,4-8°C保存运输,血液样本尽量在8小时内进行有核细胞分离,最长不超过12小时。 |
|
积液类样本,腹⽔,胸腔积液,膝盖积液,淋巴液,灌洗液和脑脊液等样本 |
≥5mL ,取样后置于4-8°C 环境进行保存运输。 |
分析内容
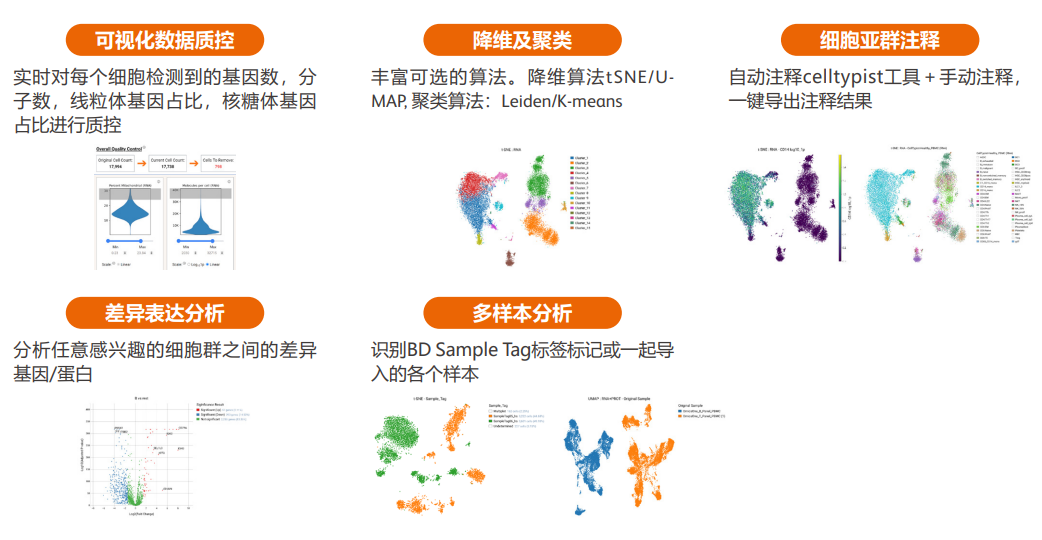
应用方向
BD 单细胞的技术平台覆盖免疫系统与疾病、肿瘤学与血液学、病原体感染与自身免疫性疾病等多个研究领域,不仅揭示了疾病机制,还推动了诊断和治疗技术的进步。从造血干细胞的研究到细胞黏附分子,从免疫检查点到共刺激分子,再到感染性疾病的检测,BD单细胞为科学研究提供了全面的支持,助力研究者深入理解疾病过程,开发更有效的治疗方法。
